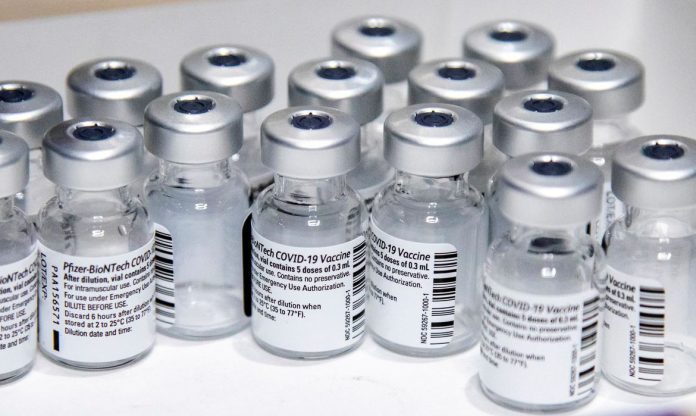
A Agência Nacional de Vigilância Sanitária (Anvisa) afirmou ter recebido as informações que solicitou à Pfizer para completar a análise do pedido de autorização de uso da vacina da fabricante para crianças de 5 a 11 anos. A vacina está registrada no Brasil desde 23 de fevereiro deste ano para pessoas com mais de 16 anos e, para a faixa etária de 12 a 15 anos, desde 11 de junho.
De acordo com a Anvisa, foram solicitados os dados de eficácia; de segurança da Coorte 2 e análises exploratórias de imunogenicidade contra a variante Delta, conforme enviado ao FDA/EUA; “dados recentes de farmacovigilância”; “discussão consubstanciada sobre o risco identificado miocardite/pericardite para crianças de 5 a <12 anos de idade, incluindo comparações (incluindo a incidência observada) com outras faixas etárias e por sexo”.
Além disso, “informações quanto as diferenças entre as ações previstas no Plano de Minimização de Riscos e de farmacovigilância encaminhado à Anvisa em relação ao aprovado pela FDA/EUA”; “relatório de miocardite e pericardite, conforme compromisso com a FDA/EUA”; e “envio de informações exigências e repostas às exigências encaminhadas pela FDA/EUA e Agência europeia de medicamentos (EMA)”.
Ainda segundo a Anvisa, por conta do pedido de mais dados e esclarecimentos, o prazo estava suspenso. A expectativa é que a agência reguladora faça análise técnica sobre o assunto e dentro de um prazo de 30 dias. Apesar de ter relatado que recebeu os dados, a agência disse que vai analisar a documentação para fazer nova uma estimativa de prazos.
Entre em nosso canal do Telegram e receba informações diárias, inclusive aos finais de semana. Acesse o link e fique por dentro: https://t.me/portalnotisul
Fonte: G1